Cet article a été traduit à l'aide du logiciel Deepl (et les visuels par Google Traduction) ; il peut persister des erreurs : merci de vous référer au texte d'origine ! De même, les tableaux déjà peu lisibles n'ont pas été traduits vu la proximité des mots entre anglais et français, et afin d’alléger l’article déjà très long, les références n’ont pas été reprises et traduites, mais la numérotation est préservée : consultez les articles sources en anglais pour vous y rapporter. Merci pour votre compréhension 😉
Dans Herbalgram, Numéro : 145, Pages : 46-67
Par Sandra Clair, PhD,(a) Ray Kirk, PhD,(a) Ian Douglass Coulter, PhD,(b) et Reinhard Saller, PhD, MD(c)
Lien vers les articles originaux :
- https://pubmed.ncbi.nlm.nih.gov/37279716/
- https://karger.com/cmr/article-abstract/30/4/340/844901/A-Pragmatic-Historical-Assessment-Tool-A-New?redirectedFrom=fulltext
(a) École des sciences de la santé, Faculté de santé, Université de Canterbury (Christchurch, Nouvelle-Zélande)
(b) Centre RAND Research Across Complementary and Integrative Health Institutions (REACH), RAND Corporation (Santa Monica, Californie) ; Université de Californie, Los Angeles (Los Angeles, Californie) ; Université des sciences de la santé de Californie du Sud (Whittier, Californie)
(c) Université de Zurich (Zürich, Suisse)
Note de la rédaction : Les analyses et les conclusions présentées dans cet article s'appuient sur la thèse de doctorat de l'auteur principal (achevée en 2019) et ont été approfondies dans un article méthodologique évalué par des pairs (2023), qui a présenté et validé un nouvel outil d'évaluation historique pragmatique (PHA).(1–3)
Abstract
Introduction : Les essais contrôlés randomisés
(ECR) sont largement considérés comme la référence réglementaire en matière
d'évaluation de la sécurité et de l'efficacité des médicaments, mais pour les
milliers d'espèces végétales utilisées dans les systèmes médicaux traditionnels
à travers le monde, de tels essais sont souvent peu pratiques, voire
irréalisables. Bien que certaines juridictions reconnaissent les preuves issues
de l'usage traditionnel, il manque souvent des lignes directrices claires pour
la compilation et l'évaluation systématiques des données historiques. Une
méthodologie structurée est nécessaire pour garantir que les indications
thérapeutiques de longue date soient documentées et évaluées de manière
cohérente, plutôt que d'être ignorées au profit d'utilisations récentes ou
vérifiées expérimentalement.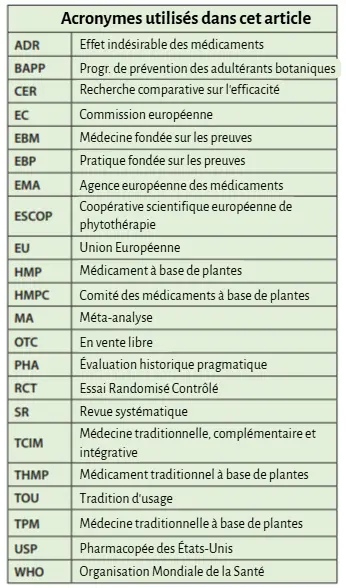
Méthodologie : Cet article présente l'outil d'évaluation historique pragmatique (PHA), un cadre systématique développé pour élargir l'éventail des sources de données utilisées pour évaluer l'efficacité et la sécurité des plantes médicinales traditionnelles (TPM) dans la materia medica européenne. S'appuyant sur la littérature médicale et réglementaire professionnelle en langue allemande couvrant 400 ans, et en prenant comme exemples l'arnica (Arnica montana, Asteraceae) et le millepertuis (Hypericum perforatum, Hypericaceae), l'outil PHA permet la validation croisée des données issues de textes médicaux historiques, de références contemporaines en phytothérapie, de pharmacopées, de monographies sur les plantes médicinales et d'études scientifiques, y compris des essais contrôlés randomisés (ECR).
Conclusion : Les conclusions des travaux de recherche de l'auteur principal révèlent une forte concordance entre les données cliniques historiques, les avals réglementaires historiques et les données scientifiques modernes, ce qui confirme la fiabilité des observations cliniques intergénérationnelles en tant que source de données crédible. L'intégration systématique de cette littérature dans des cadres réglementaires fondés sur des données probantes peut améliorer les évaluations de la TPM et élargir l'accès à des thérapies sûres et validées par l'histoire. Bien que l'outil PHA ait été développé à partir de sources européennes, il offre un modèle pouvant être adapté et validé pour d'autres traditions médicales écrites à travers le monde.
Note terminologique : Pourquoi « médicaments traditionnels à base de plantes » ? Les auteurs utilisent le terme « médicaments traditionnels à base de plantes » (TPM) car d’autres appellations courantes peuvent prêter à confusion ou être trop générales. Par exemple, les catégories de l’OMS « médecines traditionnelles » (MT) et « Médecines traditionnelles, complémentaires et intégrative » (TCIM) englobent de nombreuses pratiques non à base de plantes, tandis que les termes européens « médicaments à base de plantes » (HMP) et « médicaments traditionnels à base de plantes » (THMP) renvoient à des catégories réglementaires spécifiques.
Introduction
Les médicaments traditionnels à base de plantes (TPM) sont des produits thérapeutiques d'origine végétale préparés et utilisés selon des pratiques médicales ancestrales. Ils constituent des remèdes essentiels dans les systèmes de médecine traditionnelle, et leur utilisation généralisée perdure depuis des millénaires, se prolongeant jusqu'au XXIe siècle. Aujourd’hui, elles sont utilisées parallèlement aux médicaments de synthèse et aux autres traitements médicaux conventionnels. La popularité durable des TPM, mise en évidence, par exemple, par le rapport 2024 Herb Market Report de l’American Botanical Council, souligne leur importance persistante.(4) Pourtant, malgré leur pertinence médicale et culturelle persistante,(5,6) l’intégration formelle des TPM dans les systèmes de santé publique contemporains — et, par conséquent, l’accès équitable des patients — a progressé lentement dans de nombreux pays.(7)
L'une des raisons de cette lenteur réside dans la complexité de la réglementation des thérapies traditionnelles dans le cadre des politiques de santé récentes fondées sur des données probantes. Les systèmes réglementaires mis en place tout au long du XXe siècle ont été conçus principalement pour encadrer les nouvelles entités chimiques de synthèse et pour trouver un équilibre entre la sécurité publique et la faisabilité pratique. Les cadres réglementaires modernes sont généralement fondés sur le risque, ce qui signifie que le niveau de surveillance est censé être proportionnel au danger potentiel que peut présenter une substance ou une pratique. Une approche fondée sur le cycle de vie est également essentielle, afin de garantir que la réglementation tienne compte de l'ensemble du cycle de vie d'un produit ou d'une pratique, depuis son développement et son autorisation jusqu'à sa surveillance à long terme. La pharmacovigilance joue un rôle crucial dans ce processus en évaluant en permanence la sécurité et l'efficacité des traitements autorisés.
Si ces éléments contribuent à la mise en place d'un cadre réglementaire solide pour les nouvelles substances, les exigences en matière de preuves élaborées pour les nouvelles substances synthétiques peuvent rendre ces cadres purement théoriques, limitant ainsi leur applicabilité aux TPM connues, qui ont évolué au fil d'une longue utilisation dans la pratique et s'appuient sur une validation médicale empirique. Les remèdes naturels à base de plantes issus des systèmes médicaux traditionnels ne s'inscrivent souvent pas parfaitement dans les modèles biomédicaux standardisés d'efficacité des médicaments, d'évaluation des risques et de surveillance réglementaire.
Bien qu'il existe de nombreux outils permettant de synthétiser les données issues d'essais contrôlés randomisés (ECR), de méta-analyses (MA) et de revues systématiques (RS)(8-12), il n'est peut-être pas possible d'appliquer ces mêmes méthodes aux MTP et à leurs utilisations holistiques dans le cadre d'un système ouvert à l'échelle de la population. De plus, dans les juridictions qui autorisent les données bibliographiques sur l'usage traditionnel dans le cadre du processus d'autorisation des médicaments, des incertitudes subsistent quant à la manière dont ces documents doivent être rassemblés et évalués, compte tenu de la diversité des réglementations et des catégories de produits.(21)
Ces lacunes soulignent la nécessité de disposer d'outils pragmatiques de compilation des données qui facilitent la collecte et l'évaluation systématiques des données historiques sur l'utilisation de la médecine traditionnelle, en particulier lorsque les données issues d'essais cliniques randomisés (ECR), d'analyses de méta-analyses et de revues systématiques sont limitées ou font défaut.
Dans sa Stratégie de l’OMS en matière de médecine traditionnelle : 2014-2023(22) et dans la version actualisée de la Stratégie mondiale de l’OMS en matière de médecine traditionnelle 2025-2034(23), l’Organisation mondiale de la santé (OMS) exhorte les gouvernements à mettre en place des cadres réglementaires favorisant l’intégration formelle des thérapies traditionnelles, y compris les MTP, dans les systèmes de santé nationaux. La Déclaration d'Astana de l'OMS (2018)(24) affirme que l'accès formel des patients aux médicaments traditionnels est essentiel pour parvenir à une couverture sanitaire universelle. Bien que les décisions en matière de politique de santé soient influencées par divers facteurs — notamment la volonté politique (ou l'absence de celle-ci) d'un gouvernement d'intégrer des méthodes de traitement complémentaires —, les preuves d'efficacité et de sécurité restent primordiales pour réintégrer les médicaments traditionnels dans les cadres réglementaires modernes.(25)
L'un des obstacles courants à l'intégration réside dans le manque perçu de données probantes à l'appui des médecines traditionnelles. Cette hypothèse peut contribuer à la lenteur de l'intégration de ces thérapies de longue date dans les systèmes de santé publique, même dans les pays qui ont adopté la Stratégie de l'OMS en matière de médecine traditionnelle : 2014-2023.(26,27) L'appel persistant en faveur des essais cliniques comme source privilégiée de données probantes pour les médicaments traditionnels non brevetés néglige à la fois le manque de ressources disponibles pour recueillir ce type de données et l'applicabilité limitée des résultats de ces essais à l'ensemble de la population de patients. Appliquer aux MTP les mêmes exigences en matière de données probantes que celles utilisées pour les interventions biomédicales novatrices et brevetables et les médicaments de synthèse risque de compromettre l'accès équitable des patients si d'autres sources de données probantes valides et disponibles ne sont pas prises en compte de manière équivalente.(28)
Typologies des données probantes en médecine
La sous-représentation des TPM sûres et efficaces dans les systèmes de santé publics soulève une question politique importante : comment les TPM, élaborées et utilisées selon des pratiques médicales ancestrales, peuvent-elles être étayées dans les cadres contemporains fondés sur les données probantes ? Cela nécessite d’examiner ce qui constitue le fondement probatoire des interventions médicamenteuses existantes et de comparer celui-ci aux données probantes étayant l’efficacité et la sécurité des TPM. Ces questions sont pertinentes car la base de données probantes des MTP est principalement de nature empirique (observationnelle).
La biomédecine occidentale s’appuyait sur des données probantes bien avant l’émergence du mouvement de la médecine fondée sur les preuves (EBM) dans les années 1990. Trois formes principales de données probantes sous-tendent la biomédecine occidentale : les données probantes empiriques (observationnelles), les données probantes physiopathologiques (expérimentales) et les données probantes issues d’essais cliniques.(29)
Les données empiriques (observationnelles) découlent d'observations cliniques répétées, réfléchies et évaluées de manière critique des interventions thérapeutiques. Par exemple, l'efficacité des préparations à base de pavot à opium (Papaver somniferum, Papaveraceae) sur la physiologie humaine, documentée depuis le Corpus Hippocraticum (vers 420–vers 320 avant notre ère), a été évaluée de cette manière empirique.
Les données physiopathologiques (expérimentales) relèvent de la recherche en laboratoire. Par exemple, la confirmation par Alexander Fleming, en 1928, des effets antibactériens de la pénicilline constitue un exemple de ce type de données.
Les données issues d'essais cliniques proviennent d'études menées chez l'homme, telles que les ECR réalisés avec des participants sélectionnés dans des conditions contrôlées. Ce type de données est généralement utilisé pour établir l'efficacité et la sécurité d'un nouveau médicament ou d'une nouvelle intervention.
Ces trois formes clés de données ne s’excluent pas mutuellement ; elles apportent plutôt des éléments de réponse à différentes questions de recherche. Bien que toutes trois contribuent à la biomédecine occidentale, les données d’observation sont aujourd’hui souvent considérées comme anecdotiques ou inférieures aux études cliniques sur l’homme, en particulier aux ECR.(30,31) Pourtant, la médecine factuelle s’appuie également sur les observations consignées et l’expérience pratique des cliniciens,(32) en particulier pour les patients multimorbides qui sont sous-représentés dans les ECR et pour les informations de sécurité issues des résultats observés chez les patients dans la pratique clinique. Ces données sont essentielles lorsque la taille de l'échantillon ou la durée d'un ECR est insuffisante pour détecter des effets indésirables à long terme ou rares.(31,33)
Si les ECR sont actuellement privilégiés dans les systèmes réglementaires occidentaux en tant que référence absolue pour l'évaluation des interventions, leurs protocoles rigoureux peuvent limiter la pertinence de leurs résultats dans la pratique clinique réelle.(34) Par exemple, des critères d'inclusion restrictifs peuvent limiter les conclusions aux personnes qui ressemblent étroitement aux participants sélectionnés (évidence interne), ce qui soulève des questions quant à la pertinence de l'intervention pour une application plus large en santé publique (validité externe). (35–37) En général, les ECR limitent leurs évaluations d'efficacité et de sécurité à une cohorte spécifique et à une durée d'essai relativement brève. Par conséquent, ils ont une valeur probante limitée pour les cliniciens traitant des patients diversifiés et sont donc souvent complétés par d'autres formes de données probantes, en particulier lorsqu'un ECR manque de validité du modèle (c'est-à-dire lorsque sa conception ne reflète pas la manière dont le traitement est généralement utilisé dans la pratique).(38–40)
Selon certaines estimations, plus de la moitié des traitements issus de la biomédecine occidentale conventionnelle, en particulier ceux destinés aux pathologies comorbides ou multimorbides, ne s’appuient pas sur des données issues d’essais cliniques randomisés (ECR), ce qui met en évidence la difficulté d’appliquer les critères de la médecine factuelle à des situations complexes rencontrées dans la pratique clinique. (41–43) Plus frappant encore, les médicaments de synthèse approuvés selon des critères stricts de médecine factuelle peuvent s’avérer beaucoup moins efficaces que prévu chez les patients dans la pratique clinique.(44) De plus, les substances nouvellement approuvées présentent parfois des effets indésirables graves, voire mortels, qui ne sont découverts qu’à l’issue de la surveillance post-commercialisation.(19,45–47)
Un autre défi lié à l'obtention de données issues d'essais cliniques randomisés (ECR) pour les interventions cliniques réside dans la difficulté à obtenir l'autorisation éthique pour mener des recherches impliquant des populations vulnérables. Des études suggèrent que les personnes s'occupant d'enfants, ainsi que certaines femmes enceintes et mères allaitantes, sont particulièrement préoccupées par la sécurité des médicaments et peuvent préférer les remèdes traditionnels, perçus comme plus sûrs et plus familiers que les produits pharmaceutiques conventionnels.(48–50) Cependant, peu d'essais cliniques sont disponibles pour étayer ces préférences. En l'absence de telles données, les autorités de réglementation peuvent appliquer le « principe de précaution » pour restreindre l'utilisation des traitements, y compris les TPM, pour ces populations. Ces restrictions sont principalement dues à un manque de données scientifiques, et non à des préoccupations de sécurité avérées. Par conséquent, les TPM peuvent ne pas être officiellement approuvées par les autorités de réglementation pour ceux qui souhaitent les utiliser, ce qui conduit les patients à acheter des remèdes tels que des compléments alimentaires, qui sont généralement réglementés selon des cadres moins stricts.
Il a donc été proposé que, dans le cadre de la pratique fondée sur les preuves (EBP), « les connaissances issues de diverses sources qui ont été soumises à des tests et jugées crédibles » (51) soient considérées comme des preuves.(33,51) Cette approche pragmatique se reflète également dans l'appel constant de l'OMS à « identifier les sources de preuves, qu'elles soient historiques, traditionnelles ou scientifiques, qui corroborent ou infirment une thérapie particulière ». (22,52)
L'usage traditionnel documenté comme élément de preuve
Depuis plus de 3 500 ans, l'usage thérapeutique des plantes médicinales est largement documenté dans les textes médicaux, pharmaceutiques et botaniques de diverses cultures, reflétant les connaissances scientifiques et médicales de l'époque. (53–55) Parmi celles-ci, la tradition médicale européenne offre un corpus textuel particulièrement riche sur l’utilisation des plantes médicinales, consigné dans des manuels de référence médicaux, des formulaires, des antidotaires, des dispensatoires, des herbiers, des monographies, ainsi que dans les pharmacopées officielles et leurs compendiums. Cet ensemble de documents correspond à la description de l'OMS d'un système de médecine traditionnelle « codifié » : il est consigné par écrit, relève du domaine public et s'est transmis de génération en génération.(58) Ce n'est qu'au XXe siècle, avec l'essor des médicaments de synthèse, que les médicaments à base de plantes ont été relégués, dans les systèmes de santé occidentaux, à des formes de traitement mineures et complémentaires.(57)
Dans les traditions médicales écrites, les inquiétudes concernant la disponibilité limitée des données issues d'essais cliniques randomisés (ECR) pour les plantes médicinales traditionnelles (PMT) occultent souvent les preuves empiriques substantielles que l'on trouve dans la littérature réglementaire internationale (par exemple, les pharmacopées, les recueils et les monographies sur les plantes médicinales publiés sous l'égide des États), ainsi que dans les textes médicaux historiques et leurs équivalents phytothérapeutiques contemporains. La littérature professionnelle sur la materia medica botanique constitue une vaste source d'observations intergénérationnelles sur l'efficacité des médicaments à base de plantes dans la pratique quotidienne, impliquant souvent un grand nombre de patients. Ces données sont empiriques et proviennent principalement de rapports de cas pragmatiques et de séries de cas documentés par des cliniciens.
Outre ces données empiriques établies de longue date, un nombre croissant d’ECR, de recherches sur l’efficacité comparative (REC) et d’essais cliniques pragmatiques (études d’efficacité en conditions réelles) vient enrichir la base de données factuelles sur les MTP. Les REC et les essais pragmatiques présentent l’avantage de générer des résultats de recherche qui reflètent les conditions réelles (33,58,59) et correspondent plus étroitement à la base de données empiriques qui sous-tend les connaissances médicales traditionnelles. Si ces études contribuent à renforcer la base de données probantes globale sur les plantes médicinales, elles ne sont pas disponibles pour de nombreuses espèces végétales utilisées dans les systèmes de médecine traditionnelle.
Certaines autorités réglementaires acceptent les données issues de la tradition d'usage (TOU) comme preuve principale pour l'autorisation des produits traditionnels à base de plantes (TPM), mais cette acceptation reste inégale d'une juridiction à l'autre.(60-63) En revanche, les pratiques actuelles de soins aux patients et les programmes universitaires en pharmacologie végétale et en pharmacie continuent de s'appuyer fortement sur des données d'observation de longue date, classées comme savoirs traditionnels (TK).(64) Ces savoirs servent également de ressource pour la recherche scientifique et les initiatives de découverte de médicaments.(65-70)
Selon une enquête publiée par l’OMS dans les années 1980, environ 75 % des 119 médicaments conventionnels largement utilisés à l’époque étaient soit dérivés de plantes médicinales, soit synthétisés à partir de composés d’origine végétale, souvent à des fins thérapeutiques identiques ou similaires à celles de la médecine traditionnelle.(71) Selon un article de revue publié en 2009, environ 40 % de tous les médicaments conventionnels modernes restent des produits naturels ou des dérivés semi-synthétiques.(72) Ce recours continu à l'expertise médicale traditionnelle pour éclairer la recherche scientifique suggère que les connaissances cliniques professionnelles de longue date sur les plantes médicinales se sont souvent révélées fiables et vérifiables.
Prévalence et nécessité des médecines traditionnelles
Le Centre mondial de l’OMS pour la médecine traditionnelle, créé en 2022, estime que dans 88 % des pays du monde, la population a recours à des médecines traditionnelles, telles que les TPM.(73) Ce recours généralisé met en évidence l’intérêt d’une approche pluraliste des soins de santé : les médicaments synthétiques modernes ne peuvent pas répondre à tous les besoins de santé, peuvent être inaccessibles ou d'un coût prohibitif pour certains, et ne sont pas toujours appropriés ou efficaces.(52,74) De plus, s'appuyer uniquement sur une approche biomédicale unique est insuffisant pour relever les défis croissants de santé publique résultant de maladies chroniques, dégénératives et liées au mode de vie, qui nécessitent des stratégies de santé plus larges.(75)
Dans certaines régions du monde, les médecines traditionnelles constituent la seule forme de soins de santé accessible.(76,77) En revanche, les consommateurs d'Europe occidentale et septentrionale (en particulier en France, en Allemagne, en Suisse, en Autriche, au Royaume-Uni et en Suède) utilisent les plantes médicinales pour compléter les traitements conventionnels, pour traiter des maladies chroniques non mortelles, pour prévenir les maladies et pour promouvoir la santé.(78–82) Dans certains pays d'Europe de l'Est, des conditions économiques difficiles et un accès limité à des produits pharmaceutiques coûteux peuvent amener les personnes à rechercher des MTP plus abordables pour leurs besoins en soins de santé primaires.(83)
L'usage médical de longue date comme fondement de la réglementation
Évolution du cadre réglementaire européen
Partout dans le monde, les autorités de réglementation sont depuis longtemps confrontées au défi de mettre en place des cadres adaptés aux TPM tout en respectant le niveau de preuve exigé par les cadres réglementaires actuels. En Europe, les autorités de réglementation ont adopté une approche pragmatique face à ces défis dès les années 1960. La directive paneuropéenne 65/65/CEE, article 4.8 a(ii), a établi une procédure simplifiée d'autorisation de mise sur le marché pour les substances naturelles et synthétiques connues, sur la base de preuves bibliographiques.(84,85) S'appuyant sur ce cadre, la directive 2004/24/CE de l'Union européenne (UE) (anciennement 2001/83/CE) a continué à reconnaître les données bibliographiques ou les données issues de l'usage traditionnel (TOU) comme preuves principales pour l'enregistrement d'ingrédients ou de produits à base de plantes dans une catégorie simplifiée.(86)
Afin de faciliter le processus d'enregistrement de certaines thérapies à base de plantes au sein de l'UE — en particulier celles pouvant être qualifiées de « médicaments traditionnels à base de plantes » (THMP) —, le Comité des médicaments à base de plantes (HMPC) a élaboré des monographies communautaires sur les plantes médicinales, favorisant ainsi la libre circulation de ces produits entre les États membres. L'établissement de ces monographies représente un investissement important de la part de l'UE pour protéger les thérapies à base de plantes traditionnelles et favoriser un accès harmonisé au marché.(87) Cependant, la brièveté de nombreuses monographies communautaires sur les plantes médicinales peut refléter les défis scientifiques et politiques de la directive européenne 2004/24/CE, qui exige que les indications autorisées, les modes d'application et les preuves d'efficacité et de sécurité (innocuité) soient déterminés par consensus. Si aucun consensus ne peut être atteint, les monographies du HMPC doivent être approuvées à la majorité absolue des représentants des États membres. Compte tenu de la diversité des points de vue sur les évaluations scientifiques, des cadres réglementaires nationaux existants et des contextes juridiques et culturels des MTP dans les États membres, il est difficile de parvenir à un consensus sur un large éventail d’indications traditionnelles, de posologies et de modes d’administration.(88,89)
Interprétation et application du critère de « longue tradition d'utilisation »
Une difficulté persistante dans la réglementation européenne relative aux MTP réside dans la définition de ce qui constitue une « longue histoire d’utilisation ». Dans le cadre du régime THMP, la directive 2004/24/CE exige des preuves documentées d’une utilisation traditionnelle s’étendant sur au moins 30 ans, dont 15 ans au sein de l’UE.(62,90,91)* Cette norme — plus courte que la référence anthropologique de trois générations (environ 75 ans)(22) — a permis à de nombreux médicaments à base de plantes en vente libre (OTC) établis de longue date de rester sur le marché de l’UE. Cependant, une interprétation strictement formaliste de ce qui qualifie un remède à base de plantes comme traditionnel (c'est-à-dire exigeant des preuves récentes et continues d'une formulation, d'une posologie et d'un format d'administration inchangés) s'est parfois avérée indûment restrictive.(92) Une telle interprétation peut exclure des remèdes traditionnels utilisés dans les États membres de l'UE depuis plus de 30 ans mais ayant subi des modifications légitimes.(93) Elle néglige également la nature dynamique de la tradition,(94,95) selon laquelle les préparations et les utilisations peuvent évoluer au fil du temps, souvent pour des raisons sans rapport avec l’efficacité (par exemple, les préférences des consommateurs, les directives de conservation, la disponibilité). Dans de telles situations, la médecine traditionnelle privilégie l’équivalence fonctionnelle et thérapeutique de l’efficacité plutôt que la stricte cohérence structurelle d’une formulation — une perspective reflétée dans la pratique réglementaire suisse et de plus en plus étayée par la pharmacologie des réseaux et la recherche sur la plasticité botanique.(96–98) Bien que les monographies communautaires de l'UE sur les plantes médicinales fournissent des aperçus régulièrement mis à jour concernant la posologie, le mode d'administration et les indications traditionnelles approuvées d'une plante, certaines plantes médicinales, préparations et indications bien documentées ne figurent toujours pas dans ces listes.
Ces deux exemples montrent comment certaines préparations et indications traditionnelles établies de longue date peuvent ne pas être prises en compte dans les monographies communautaires actuelles de l'UE sur les plantes médicinales :
Arnica (Arnica montana, Asteraceae) : Les extraits traditionnels à base d'eau et d'huile de fleurs d'arnica ont été autorisés dans plusieurs éditions du Deutsches Arzneibuch (Pharmacopée allemande) et dans des recueils connexes, ainsi que dans la monographie Arnicae flos de la Commission E allemande (1984).(99,100) Ces textes réglementaires ont servi de base à l'autorisation de mise sur le marché des produits thérapeutiques à base de plantes en Allemagne avant l'élaboration des monographies communautaires communes de l'UE sur les plantes médicinales. La littérature médicale historique examinée pour cet article contient également de nombreuses références à ces préparations utilisées en pratique clinique.(101)
Cependant, la monographie communautaire finale sur la fleur d’arnica ne les a pas incluses.(102) Le rapport d’évaluation n’a pas cité les préparations officielles décrites dans le Deutsches Arzneibuch, la monographie de la Commission E ou des sources réglementaires comparables d’autres États membres, et n’a pas non plus évalué systématiquement les preuves intergénérationnelles issues de textes médicaux historiques et de manuels contemporains (preuves empiriques). Au lieu de cela, il a conclu que les préparations exclues ne répondaient pas aux exigences de la directive.(103)
Millepertuis (Hypericum perforatum, Hypericaceae) : Les manuels spécialisés sur la pharmacopée européenne recommandent systématiquement le millepertuis pour le traitement des traumatismes contondants et pénétrants touchant le système musculo-squelettique et les nerfs (notamment les entorses, les élongations, les contusions, les inflammations et les douleurs), ainsi que pour soulager les troubles liés aux affections rhumatismales et aux troubles menstruels (tableau 1). La monographie de la Commission E sur Hyperici herba (1984) reconnaissait de même les effets thérapeutiques de la plante sur le système musculo-squelettique dans les blessures aiguës et liées à des contusions, ainsi que dans les myalgies (douleurs musculaires).(100,104) Cependant, la monographie communautaire de 2009 sur le millepertuis et sa révision de 2022 omettent ces indications, malgré des siècles de documentation et des preuves préliminaires modernes à l’appui.(101,105–108)
L'intégration d'évaluations
historiques systématiques de l'usage traditionnel (TOU) dans la mise en œuvre
de la directive européenne 2004/24/CE pourrait contribuer à garantir une
représentation plus complète des thérapies à base de plantes traditionnelles au
sein de la tradition médicale européenne, rendant ainsi l'enregistrement en
vertu de ces réglementations plus réalisable.(1,93,10)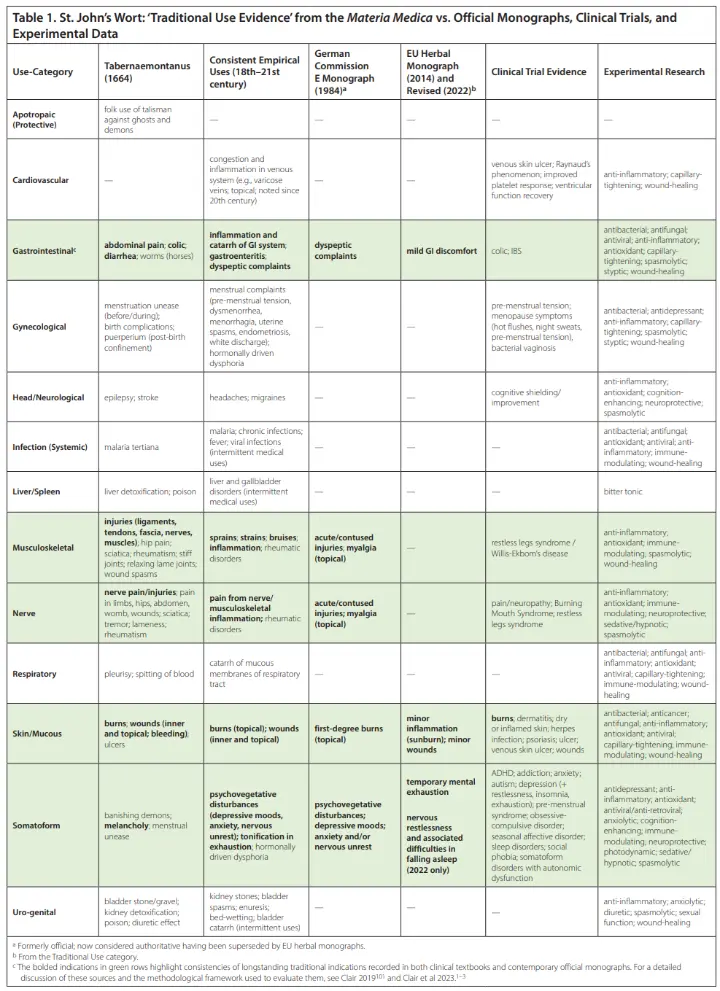
Allégations autorisées et implications pour le marché
Un autre aspect essentiel de la réglementation relative aux MTP réside dans le champ d'application des allégations d'usage traditionnel autorisées. Si aucune autorité réglementaire occidentale n'autorise les allégations d'usage traditionnel pour des maladies ou des affections graves en l'absence d'essais cliniques randomisés, certaines autorisent des allégations allant au-delà du maintien ou de la promotion de la santé. Dans l'Union européenne, en revanche, les allégations d'usage traditionnel sont limitées aux affections bénignes pouvant faire l'objet d'un autodiagnostic et d'une automédication.(90)
La portée restreinte des allégations de santé autorisées pour les MTP en vertu de la directive 2004/24/CE, combinée aux normes de fabrication de qualité pharmaceutique et à la liste restreinte d’utilisations traditionnelles et de préparations pré-approuvées, a probablement entravé une adoption plus large de cette voie d’autorisation de mise sur le marché.(109) Après la mise en œuvre de la directive, de nombreux remèdes traditionnels, en particulier ceux provenant des petits États membres de l’UE, ont disparu du marché.(93) En conséquence, de nombreuses entreprises ont préféré enregistrer leurs médicaments à base de plantes en tant que compléments alimentaires, soumis à une réglementation alimentaire moins stricte. Cependant, les produits classés comme compléments alimentaires à base de plantes ne peuvent pas faire l’objet d’allégations d’usage traditionnel en vertu du règlement (CE) n° 1924/2006 de l’UE concernant les allégations nutritionnelles et de santé. Cette restriction signifie que les consommateurs ne peuvent souvent pas consulter les informations relatives aux usages traditionnels sur les produits, ce qui rend plus difficile un choix éclairé.(110)
Évaluation systématique des données relatives à l'usage traditionnel à l'aide de l'outil d'évaluation historique pragmatique
Afin de pallier les lacunes dans la collecte et l'évaluation des données relatives à l'usage traditionnel à des fins réglementaires, nous avons développé l'outil PHA, conçu pour rassembler et synthétiser de manière systématique les indications traditionnelles établies de longue date.
L'outil PHA a été initialement développé et testé dans le cadre de la thèse de doctorat d'un des auteurs de cet article (SC) à l'université de Canterbury, en Nouvelle-Zélande (2019)(101), puis dans un article méthodologique évalué par des pairs publié dans Complementary Medicine Research (2023).(1–3) Le présent article s'appuie sur ces travaux en appliquant l'outil PHA pour évaluer comment les données intergénérationnelles sur l'usage traditionnel peuvent éclairer le cadre réglementaire européen relatif aux produits traditionnels médicinaux (TPM).
Depuis un certain temps, les chercheurs reconnaissent l'importance des données bibliographiques pour comprendre les propriétés pharmacologiques des plantes médicinales, mais leur valeur potentielle dans le cadre des évaluations réglementaires a fait l'objet de moins d'attention.(30,68,85,93, 111–119) Bien que les données bibliographiques étayant les allégations d'usage traditionnel soient légalement reconnues dans certains systèmes réglementaires occidentaux (par exemple, dans l'UE, en Suisse, au Canada et en Australie), les orientations sur la manière de rassembler et de présenter systématiquement des sources admissibles autres que les pharmacopées et les monographies officielles restent limitées. L'admissibilité des manuels médicaux cliniques sur la materia medica traditionnelle est particulièrement floue : si certains organismes de réglementation reconnaissent ces textes comme des preuves valables, rares sont ceux qui précisent comment évaluer leur pertinence ou leur fiabilité.(120) Certaines juridictions, comme la Nouvelle-Zélande, ont totalement ignoré la littérature clinique professionnelle en tant que source de preuves dans leurs efforts de longue date pour réglementer les TPM.(121)
Pour que les données bibliographiques soient jugées recevables en vue de l'enregistrement d'un produit à base de plantes, les données historiques doivent faire l'objet d'une évaluation critique quant à leur pertinence et leur validité. En l'absence de critères clairs concernant les sources recevables ou d'une méthode cohérente pour compiler les données relatives à l'usage traditionnel, de nombreuses indications traditionnelles de longue date risquent d'être négligées, comme en témoigne la portée limitée des allégations pré-approuvées dans les monographies communautaires de l'UE sur les plantes médicinales. Il est de plus en plus reconnu que les diverses utilisations historiques des plantes médicinales ne sont pas arbitraires, mais reposent au contraire sur leur capacité à exercer de multiples actions pharmacologiques distinctes.(122,123) La mise en place d’un cadre systématique pour la collecte et l’évaluation de ces preuves peut contribuer à garantir que l’ensemble des utilisations traditionnelles de longue date d’une plante soit reconnu au sein des systèmes réglementaires contemporains.(30,101)
Lors du développement et de la mise à l'essai de l'outil PHA, nous avons utilisé de multiples sources qualitatives et quantitatives pour comparer et vérifier les données relatives aux usages médicaux traditionnels faisant l'objet de l'étude — une approche appelée triangulation.(124) Cette approche offre des perspectives complémentaires pour examiner un même phénomène et contribue à renforcer la fiabilité des résultats.(125)
La carte des processus PHA résume les principales étapes de cette approche :
- Sélectionner des sources bibliographiques représentatives pour une plante médicinale en utilisant des critères d'inclusion prédéfinis (tableau 2).
- Définir des catégories d'usage thérapeutique pour le codage des informations thérapeutiques.(1,2)
- Attribuer chaque indication d'une plante médicinale, issue de chaque source sélectionnée, à la catégorie d'usage thérapeutique correspondante et la reporter dans une matrice d'extraction de données.
- Analyser la cohérence de la validation médicale pour chaque indication au fil du temps, ainsi que l'efficacité et la sécurité rapportées (analyse longitudinale systématique†).
- Recouper ces résultats avec la littérature reconnue dans les cadres réglementaires allemands et européens au sens large du XIXe au XXIe siècle, ainsi qu'avec les essais cliniques disponibles et les données expérimentales à l'appui.
Validation et conception des études de cas
L'outil PHA souligne l'importance cruciale de sélectionner des sources bibliographiques à la fois représentatives et rigoureuses sur le plan méthodologique. Un critère essentiel pour que les manuels médicaux soient considérés comme recevables est qu'ils reflètent fidèlement la pratique clinique contemporaine et qu'ils documentent les évaluations des auteurs concernant les résultats thérapeutiques accumulés au cours de leur carrière professionnelle. La force des textes cliniques réside dans le fait qu'ils s'appuient sur la prise en charge réelle des patients, où les informations ont été testées, affinées et corrigées au fil du temps.
Par conséquent, les sources bibliographiques utilisées à des fins réglementaires doivent être rédigées par des praticiens ayant suivi une formation officielle et possédant une expérience clinique substantielle, ce qui confère de la crédibilité aux observations cliniques consignées dans ces textes. On accorde généralement plus de poids à ces preuves qu'aux informations reproduites dans des textes dépourvus d'évaluation clinique directe (parfois appelées « échos bibliographiques », un terme attribué à l'auteur, photographe et expert en herboristerie Steven Foster [1957–2022]).(126)
Enfin, l'établissement d'une nomenclature scientifique correcte pour une plante médicinale est essentiel pour garantir la validité des résultats de la recherche et doit tenir compte de l'évolution historique des paradigmes linguistiques, botaniques et médicaux.(3,127–129)
Grâce à une triangulation approfondie, nous avons cherché à déterminer si la littérature médicale spécialisée sélectionnée sur la materia medica européenne (rédigée par des générations successives de cliniciens ayant suivi une formation officielle) fournit des preuves fiables et vérifiables pour étayer les usages traditionnels des TPM. De telles preuves pourraient étayer la reconnaissance de ces indications thérapeutiques en vue d'une autorisation de mise sur le marché, parallèlement à d'autres sources bibliographiques reconnues, notamment les pharmacopées et les monographies sur les plantes médicinales rédigées par des organismes experts.
La « materia medica » européenne professionnelle a été choisie comme étude de cas car elle incarne un savoir clinique transmis de génération en génération au sein d’une tradition médicale codifiée, définie sur le plan géographique et culturel, qui recourait officiellement aux plantes médicinales et s’inscrivait dans les cadres établis de la pratique médicale conventionnelle et des systèmes réglementaires régionaux (tableau 2). L'analyse textuelle comparative longitudinale s'est concentrée sur la littérature en langue allemande et a débuté par ce qui est largement considéré comme le manuel médical le plus complet du XVIIe siècle, le New vollkommen Kräuter-Buch (Nouveau livre complet sur les plantes médicinales), rédigé par le médecin, apothicaire et botaniste allemand Jacobus Theodorus (latinisé sous le nom de Tabernaemontanus ; 1522–1590), et s’est achevée par les manuels de phytothérapie faisant autorité à l’heure actuelle.(130) Les sources sélectionnées servent d’exemples représentatifs répondant aux critères d’inclusion, plutôt que de constituer une liste exhaustive de toutes les données éligibles.
Après des tests préliminaires de l’outil PHA sur 13 plantes médicinales,(101) celui-ci a été utilisé pour rassembler et analyser de manière systématique les données pharmacologiques et pharmaceutiques sur l’arnica et le millepertuis. Ces plantes ont été choisies en raison de l’importance et de la notoriété des recherches scientifiques qui leur sont consacrées.
L'ensemble des données issues de la littérature spécialisée a ensuite été recoupé avec les indications thérapeutiques répertoriées dans les pharmacopées prussiennes et allemandes indépendantes, financées par l'État, ainsi que dans leurs commentaires (toutes éditions confondues), et dans plusieurs monographies modernes faisant autorité en matière de plantes médicinales. Les monographies officielles comprenaient les monographies de la Commission E allemande(99,100,104) et les monographies communautaires de l'UE sur les plantes médicinales.(102,105) Les monographies faisant autorité comprenaient les monographies de l'OMS sur les plantes médicinales,(131,132) les monographies de la Coopérative scientifique européenne de phytothérapie (ESCOP),(133,134) et celles publiées dans HagerROM — la version numérique mise à jour du manuel de référence Hagers Handbuch der Drogen und Arzneistoffe (Manuel Hager des médicaments et des substances médicinales).(135,136)
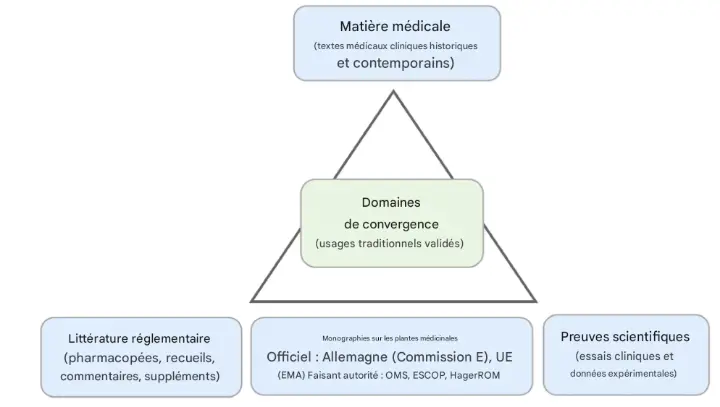
Les résultats de ces analyses bibliographiques ont ensuite été validés par recoupement avec des données cliniques et expérimentales, notamment les résultats d’ECR et les données de recherche en laboratoire, dans la mesure où celles-ci étaient disponibles (Figure 1). Les études scientifiques sur l’arnica et le millepertuis ont été identifiées grâce à des recherches systématiques dans les bases de données Medline, Embase, Allied and Complementary Medicine Database (AMED), Cochrane Library, Web of Science et Cumulative Index to Nursing and Allied Health Literature (CINAHL), puis complétées par des recherches bibliographiques manuelles.(137) Cette triangulation des données qualitatives et quantitatives a contribué à renforcer la validité des conclusions tirées de l’analyse.(124,125)
Concordance entre les indications thérapeutiques historiques et contemporaines de l’arnica et du millepertuis
L’analyse textuelle comparative longitudinale de l’arnica et du millepertuis a révélé une forte concordance entre les principales indications thérapeutiques issues de siècles de pratique clinique et celles documentées dans les pharmacopées officielles et leurs commentaires normatifs (au moins jusqu’au milieu des années 1980), les monographies modernes sur les plantes médicinales et, lorsqu’elles sont disponibles, les essais cliniques randomisés (ECR). Cette triangulation des sources phytothérapeutiques a confirmé que les principales utilisations thérapeutiques de ces deux plantes ont été rapportées de manière cohérente dans les ensembles de données tant qualitatifs que quantitatifs et ont persisté malgré les changements de paradigme majeurs dans la théorie médicale, passant des concepts humoraux à la pathologie cellulaire et à la biomédecine occidentale moderne.(57)
En ce qui concerne la fleur d’arnica et ses préparations, la littérature médicale et la littérature triangulée font état d’une transmission ininterrompue de deux grands groupes d’indications depuis plus de 400 ans dans toutes les sources historiques et contemporaines : (1) le traitement des traumatismes et des lésions du système musculo-squelettique (notamment les entorses, les foulures, les déchirures musculaires et ligamentaires, les contusions, les œdèmes et les hématomes) et (2) les douleurs associées.
De même, la triangulation à base de plantes concernant la fleur de millepertuis et ses préparations a montré une concordance entre trois groupes de troubles de santé (selon la terminologie actuelle) : (1) inflammation et catarrhe du système gastro-intestinal (par exemple, gastro-entérite, troubles dyspeptiques) ; (2) les brûlures et les plaies ; et (3) les troubles somatoformes, y compris les humeurs dépressives, l'anxiété, l'agitation nerveuse et la dysphorie d'origine hormonale liée au cycle menstruel (tableau 1).
Lorsqu’ils étaient disponibles, les résultats des essais cliniques ont confirmé la validité de ces indications traditionnelles historiques. Il convient de noter que les ECR qui respectaient les paramètres d’utilisation traditionnelle dans leur protocole d’essai (par exemple, préparations, posologies et indications comparables) donnaient généralement des résultats positifs, tandis que les ECR s’écartant des paramètres traditionnels aboutissaient parfois à des résultats contradictoires.101 Les données de la recherche expérimentale ont permis de mieux comprendre les constituants actifs et les mécanismes d’action possibles liés aux effets observés. La forte concordance entre les données historiques et modernes reflète probablement la fiabilité et la fréquence de ces effets thérapeutiques dans la prise en charge des patients au fil du temps.
Bien que seul un nombre limité de plantes ait été analysé au cours de la période de 400 ans examinée dans la thèse, la littérature clinique spécialisée sur la materia medica européenne s'est révélée à la fois fiable et exhaustive, couvrant un champ thérapeutique plus large que les documents trouvés dans les pharmacopées prussiennes et allemandes, leurs commentaires, les monographies sur les plantes médicinales des XXe et XXIe siècles, ou la recherche scientifique. Les traitements qui ont démontré leur efficacité ont été maintenus et transmis, tandis que ceux qui ne présentaient pas de valeur clinique constante (par exemple, l'utilisation de l'arnica pour le paludisme) ont finalement été abandonnés.
En revanche, les autorités réglementaires ont parfois retiré une plante, une partie de plante ou une application de l'usage thérapeutique officiel, mais pas toujours en raison d'un manque d'efficacité. Les changements paradigmatiques survenus en médecine au cours du XIXe siècle ont conduit à une moindre acceptation des données d’observation au profit de la validation expérimentale.(138) Par exemple, l’incapacité à expliquer le ou les modes d’action des préparations à base de millepertuis a conduit à l’omission de cette plante de la pharmacopée allemande du milieu du XIXe siècle jusqu’en 1986, date à laquelle les preuves irréfutables de son efficacité clinique ne pouvaient plus être niées.(101) De plus, de nombreux remèdes traditionnels ont été remplacés par des analogues synthétiques à mesure que les préférences thérapeutiques se sont tournées vers les médicaments conventionnels.(139) D’autres retraits réglementaires ont été motivés par des préoccupations liées à la conservation ou à la sécurité. Par exemple, l’autorité réglementaire allemande a interdit l’utilisation de la racine d’arnica et les indications associées pour les infections entériques à la fin du XIXe siècle en raison du statut d’espèce menacée de la plante. Plus tard, au milieu des années 1980, la Commission E a retiré de la liste l’usage interne de l’arnica (y compris les teintures traditionnelles à faible dose) en raison de préoccupations concernant des surdosages accidentels potentiels dans le cadre de la vente libre, plutôt que sur la base de preuves de risque à la posologie précédemment approuvée par les autorités de réglementation. Les interruptions réglementaires temporaires dans la transmission d'usages traditionnels de longue date devraient être évaluées au cas par cas dans le cadre des réévaluations en cours des pratiques médicinales traditionnelles (PMT).(101)
Évaluations réglementaires de la sécurité
Les considérations relatives à la sécurité font partie intégrante du processus d'autorisation réglementaire de tous les médicaments. Cependant, il n'existe aucun cadre d'évaluation de la sécurité internationalement reconnu ou normalisé pour les produits à base de plantes médicinales (TPM), car les exigences réglementaires varient d'une juridiction à l'autre. Les données modernes sur la sécurité des plantes médicinales sont désormais rassemblées à l'échelle internationale dans des bases de données de pharmacovigilance, mais les préoccupations en matière de sécurité ne sont pas propres aux systèmes réglementaires actuels. Elles sont depuis longtemps au cœur de la pratique clinique des plantes médicinales.(101)
Fondements historiques de la sécurité
Les textes médicaux historiques professionnels constituent des référentiels d'observations cliniques directes sur les plantes médicinales, y compris celles susceptibles de causer des effets indésirables (par exemple, une irritation cutanée ou une toxicité systémique en cas d'usage interne). Dès le Ier siècle, le médecin militaire grec Dioscoride (vers 40 – vers 90) a documenté des préoccupations telles que la falsification, la substitution et les effets toxiques dans son De Materia Medica, et ces informations ont été transmises au fil des millénaires.(140,141)
Les manuels médicaux du début de l'époque moderne (vers 1450–1800) et au-delà révèlent en outre la diversité des approches adoptées par les médecins pour garantir une utilisation sûre des plantes médicinales. Il s'agissait notamment d'éviter les plantes ou parties de plantes connues pour leur toxicité, de respecter les limites de dosage pour les plantes contenant des principes actifs puissants, d'associer certaines plantes afin de neutraliser les irritations potentielles et autres effets indésirables, et de choisir des méthodes d'extraction minimisant la libération de substances potentiellement nocives telles que certains alcaloïdes.(101)
Évolution au XXe siècle
À partir du XXe siècle, la sécurité des patients est restée une priorité absolue dans la littérature moderne sur la phytothérapie. La trilogie sur les plantes médicinales rédigée par Ludwig Kroeber (1872–1951), directeur de la pharmacie de l’hôpital Schwabing de Munich et membre de la Commission allemande de la pharmacopée, illustre cette prise de conscience professionnelle quant à l’utilisation sûre des plantes médicinales dans les soins cliniques.(142–144) Ses ouvrages de référence ont servi de ressources académiques pour les cours de phytothérapie de niveau universitaire jusque dans les années 1970 et continuent de fournir de précieuses informations en matière de sécurité.(145)
Les médecins et les experts en phytothérapie d’aujourd’hui restent vigilants et enregistrent systématiquement des données épidémiologiques et d’observation. Celles-ci comprennent des données ambulatoires collectées, par exemple, dans la base de données du système d’information allemand de phytovigilance (PhytoVIS) et par le Réseau européen des centres de pharmacoépidémiologie et de pharmacovigilance (ENCePP). De nombreuses organisations à travers le monde, telles que la United States Pharmacopeial Convention (USP), publient également des analyses sur la santé et la sécurité des ingrédients des compléments alimentaires, y compris les plantes médicinales.(146)
Défis actuels et approches préventives
L'une des principales limites à l'obtention d'informations sur la sécurité à partir de la littérature médicale antérieure au XXe siècle réside dans la méconnaissance des substances toxiques cumulatives (par exemple, les acides aristolochiques) présentes dans un petit nombre de plantes médicinales — des risques qui n'ont été identifiés que plus tard, et un défi qui n'est pas propre aux plantes médicinales.(147) Une autre limite tient à la reconnaissance plus récente des interactions entre les plantes médicinales et les médicaments. Pour ces raisons, les bases de données nationales et internationales de pharmacovigilance, ainsi que les systèmes dédiés post-autorisation de mise sur le marché tels que la base de données EudraVigilance (EVDAS), sont essentiels pour surveiller les effets indésirables des médicaments (EIM), y compris ceux associés aux médicaments à base de plantes.
La plus grande base de données sur les effets indésirables signalés est la VigiBase de l’OMS, gérée depuis les années 1970 par le Centre de surveillance d’Uppsala (UMC) en Suède. (148) La faible incidence des effets indésirables liés aux MTP correctement fabriqués dans l’UE (et aux remèdes à base de plantes disponibles au niveau national en général), combinée à une utilisation et une satisfaction des consommateurs à long terme, suggère que ces produits sont bien tolérés dans la pratique clinique traditionnelle européenne.(117) Malgré un risque de sous-déclaration, il est peu probable que des événements graves se produisant de manière répétée au sein de larges populations soient passés inaperçus.
Les études toxicologiques peuvent s’avérer superflues pour les substances dont l’usage traditionnel est bien documenté et pour lesquelles il existe des preuves suffisantes d’efficacité et de sécurité. Elles ne sont pas toujours exigées par les autorités de réglementation dans certaines juridictions, par exemple en Suisse et au Canada.(62,149)
Étude de cas : l’arnica
Les cadres réglementaires se concentrent souvent sur les risques potentiels associés aux substances à base de plantes, tout en négligeant parfois le fait que, dans la pratique traditionnelle, les MTP peuvent être administrées différemment et à des doses nettement plus faibles. L'auto-administration de remèdes pose un défi de taille aux traditions établies de longue date en raison de l'absence de surveillance réglementaire et de contrôle sur la manière dont les individus utilisent les produits thérapeutiques dans un cadre privé. Par conséquent, les réglementations conçues pour atténuer les risques liés à l'auto-administration peuvent involontairement exclure les pratiques traditionnelles, même parmi ceux qui possèdent les connaissances et l'expertise requises.
Le retrait de l'Arnica montana de la liste des plantes autorisées pour usage interne par la Commission E au milieu des années 1980 — malgré plus de 400 ans d'utilisation professionnelle ininterrompue de préparations à faible dose — illustre bien ce dilemme réglementaire. Les années 1980 ont marqué un tournant dans l’évaluation des risques liés aux plantes médicinales, avec l’adoption d’une nouvelle approche préventive en matière de santé publique et une tolérance moindre à l’égard de tout risque potentiel associé aux médicaments à base de plantes. La décision de la Commission E de retirer l’Arnica montana de la liste des plantes autorisées pour usage interne était largement motivée par la crainte de surdosages accidentels dans le cadre de la vente libre, plutôt que par des preuves de nocivité dans un contexte professionnel.
Cette décision a été prise malgré l’opposition de membres éminents du comité, dont le médecin et expert en plantes médicinales R. F. Weiss, qui a soutenu que la décision finale reflétait une surestimation moderne de la toxicité de l’arnica par rapport aux nombreuses preuves historiques de son innocuité et de ses bienfaits lorsqu’elle est utilisée de manière appropriée.(150)
Les rapports d'évaluation ultérieurs de la monographie européenne sur les plantes médicinales concernant Arnica montana L., flos,(103,151) ainsi que la recherche bibliographique approfondie menée par les auteurs de cet article, n'ont trouvé aucune preuve que l'usage interne traditionnel à faible dose de l'arnica (généralement 1 g ou moins) ait causé des effets indésirables graves chez des personnes ne présentant pas d'allergie à la plante.(101,137) En revanche, les données de pharmacovigilance indiquent que des effets indésirables peuvent résulter d'un surdosage, d'une utilisation excessive ou de réactions allergiques, lesquels peuvent être atténués de manière appropriée grâce à des recommandations réglementaires claires.(151)
Concilier sécurité et accès
Une solution possible pour résoudre le conflit entre l'approche de précaution des systèmes réglementaires modernes et la préservation des pratiques médicales traditionnelles de longue date consiste à classer les produits traditionnels à base de plantes (TPM) en différentes catégories réglementaires. Celles-ci pourraient inclure les produits en vente libre (OTC), avec ou sans restriction spécifique, et les remèdes réservés aux praticiens, disponibles avec ou sans certaines restrictions. Cette approche a déjà été mise en œuvre dans certaines juridictions, notamment au Royaume-Uni et en Australie.
Assurance de la qualité
Aujourd'hui, la plupart des risques associés aux préparations à base de plantes découlent d'une fabrication inadéquate ou de mesures de contrôle de la qualité insuffisantes, plutôt que des activités pharmacologiques des ingrédients et préparations à base de plantes utilisés traditionnellement.(152,153) À ce titre, les autorités sanitaires internationales et les organisations professionnelles mettent l'accent sur des normes strictes de contrôle de la qualité pour les MTP, en particulier le respect des bonnes pratiques de fabrication et des mesures d'authentification visant à prévenir l'adultération et la contamination.
Lorsqu'une préparation à base de plantes traditionnelle est fabriquée conformément à des normes de qualité établies et étayée par des données bibliographiques adéquates confirmant son innocuité dans des conditions normales d'utilisation, elle est généralement éligible à une autorisation dans le cadre des dispositifs réglementaires établis pour les TPM.(60,62,90,149)
Discussion et implications
Comme indiqué précédemment, les analyses et les conclusions présentées ici s’inspirent de la thèse de doctorat de l’auteur principal, publiée en 2019, ainsi que d’un article méthodologique évalué par des pairs, publié en 2023, qui a permis de développer et de tester l’outil PHA. Ces travaux contribuent au débat actuel sur les politiques de santé concernant l’élaboration de cadres réglementaires pragmatiques et fondés sur des preuves pour la validation des plantes médicinales utilisées traditionnellement. En démontrant que les manuels de phytothérapie historiques et contemporains peuvent constituer des sources fiables de données probantes sur l’efficacité et la sécurité des MTP dans la tradition médicale européenne, cette recherche met en évidence la valeur durable des connaissances expertes intergénérationnelles fondées sur la pratique. Cet ensemble de données empiriques, parfois validées par des ECR contemporains, représente l’un des recueils les plus complets sur l’usage thérapeutique des plantes dans la materia medica européenne.
L'outil PHA offre un cadre systématique et transparent pour la collecte et l'évaluation des données empiriques, constituant ainsi un moyen prometteur et efficace d'élargir les types de données utilisées pour valider et intégrer les MTP au sein des systèmes réglementaires modernes. Il a notamment permis d'identifier des données clés manquantes concernant la réglementation européenne en matière d'accès au marché. Le projet de révision (2025) de la monographie communautaire de l'UE sur l'Arnica montana flos(154) corrobore les conclusions de cette étude selon lesquelles la monographie de 2014 était trop prudente et incomplète dans la documentation des préparations et indications traditionnelles établies. L'évaluation actualisée du HMPC reconnaît des utilisations traditionnelles supplémentaires — telles que le traitement topique de l'inflammation due aux piqûres d'insectes et aux petits furoncles — et recommande aux États membres de reconnaître ces indications, ainsi que les extraits aqueux et huileux d'arnica précédemment omis.(151) Toutes ces omissions, et d'autres, ont été identifiées grâce à l'outil PHA.(101)
L'approche par triangulation a également démontré que l'outil PHA est efficace même lorsqu'il est appliqué à une période de compilation bibliographique plus courte que les 400 ans initialement étudiés. Pour la materia medica européenne, la combinaison d’une référence historique fondamentale (par exemple, le Nouveau livre complet sur les herbes de Tabernaemontanus) avec des manuels cliniques faisant autorité, rédigés par au moins trois générations successives de cliniciens à partir du début du XXe siècle, a suffi à corroborer les usages médicinaux historiques et à saisir les applications thérapeutiques plus récentes. Ce cadre temporel condensé s’aligne sur les priorités réglementaires de faisabilité, de praticabilité et d’efficacité.
Sur la base de ces conclusions, les auteurs de cet article proposent une approche réglementaire selon laquelle une indication traditionnelle peut être approuvée si l'une des conditions suivantes est remplie grâce à une compilation systématique de la littérature :
L'indication a été soutenue de manière constante par au moins trois générations d'experts cliniciens en phytothérapie ayant suivi une formation professionnelle, représentant trois sources faisant autorité, indépendantes et orientées vers la pratique clinique, sur une période d'au moins 30 ans ; ou l'indication a été approuvée de manière intermittente par trois générations de cliniciens en phytothérapie ayant suivi une formation et reste plausible au regard de l'usage thérapeutique actuel ou de la recherche scientifique moderne.
La deuxième condition tient compte des interruptions temporaires de la transmission, qui peuvent survenir pour des raisons sans rapport avec l'efficacité clinique. On peut citer comme exemple le retrait historique de la racine d’arnica de la pharmacopée allemande à la fin du XIXe siècle en raison d’une surexploitation, malgré sa valeur clinique persistante, ainsi que l’omission du millepertuis de la pharmacopée allemande jusqu’en 1986, en raison de l’incapacité à expliquer son ou ses modes d’action.
L'établissement de critères de sélection clairs pour les sources bibliographiques autorisées peut réduire considérablement le risque de demandes d'autorisation fondées sur des indications traditionnelles non étayées.(1) En outre, l'élargissement de la portée des indications traditionnelles autorisées au-delà des affections mineures pour inclure des affections courantes et chroniques ne mettant pas la vie en danger refléterait plus fidèlement l'étendue thérapeutique des systèmes médicaux traditionnels. Une telle approche renforcerait non seulement la pertinence des cadres réglementaires pour les MTP, mais favoriserait également un choix éclairé de la part des patients, en particulier dans les contextes où les options de soins conventionnels sont limitées ou insuffisantes.
Bien qu'aucun produit thérapeutique ne soit totalement exempt de risques, il est à la fois justifié et nécessaire que les données de sécurité issues de l'usage traditionnel (TOU) soient systématiquement intégrées à l'ensemble des données disponibles concernant les plantes médicinales.(115,155–158) Afin de garantir la pertinence clinique, les évaluations réglementaires de la sécurité devraient prendre en compte les formes de préparation et les posologies traditionnelles utilisées de génération en génération dans la pratique clinique formelle. Pour les agents thérapeutiques ayant une longue histoire d'utilisation sûre et ne faisant l'objet d'aucun rapport de pharmacovigilance négatif, des études toxicologiques expérimentales peuvent ne pas être nécessaires pour l'enregistrement sur le marché dans certaines juridictions, ce qui reflète une approche réglementaire pragmatique, fondée sur les risques et s'appuyant sur des preuves empiriques.
Il est essentiel de tester davantage l'outil PHA sur un éventail plus large de plantes médicinales traditionnellement utilisées et de contextes culturels afin de confirmer sa fiabilité et d'étendre son applicabilité. Bien que la recherche doctorale se soit concentrée sur la materia medica européenne, le cadre réglementaire proposé pourrait être adapté à d'autres traditions médicales codifiées par écrit, telles que l'Ayurveda, la médecine traditionnelle chinoise, la médecine tibétaine et d'autres. Avec des modifications appropriées, cette approche systématique pourrait faciliter la collecte de données probantes solides dans divers systèmes médicaux, à condition que des textes de référence faisant autorité et documentant des applications thérapeutiques validées puissent être identifiés. L'adoption généralisée de méthodologies rigoureuses et fondées sur des données probantes, telles que l'outil PHA destiné à la collecte et à l'évaluation systématiques des données bibliographiques historiques sur l'usage clinique traditionnel, permettra de parvenir à une harmonisation internationale des procédures réglementaires relatives aux produits traditionnels médicinaux (PTM), conformément à la directive de l'OMS. Pour les traditions orales, telles que la médecine traditionnelle maorie (Rongoā Māori) en Nouvelle-Zélande, un cadre alternatif de collecte de données s'appuyant sur l'ethnobotanique et l'ethnomédecine et guidé par des considérations culturelles et éthiques appropriées (notamment la protection de la propriété intellectuelle et le respect des systèmes de connaissances autochtones) serait nécessaire.
Idéalement, un référentiel en libre accès des indications thérapeutiques traditionnelles, compilé à partir de manuels de référence cliniques répondant à des critères établis, devrait être développé pour étayer les allégations d'usage thérapeutique des MTP dans les contextes réglementaires. La collaboration entre les régulateurs, les chercheurs et les praticiens sera essentielle pour mettre en place un tel référentiel, et l'utilisation stratégique et judicieuse de l'intelligence artificielle (IA) pourrait accélérer davantage la compilation des données issues de textes de référence médicaux validés provenant de divers systèmes médicaux, soutenant ainsi les évaluations d'experts humains à l'avenir.(159)
Conclusion
Ce travail contribue au débat sur l'élaboration de cadres de données pragmatiques destinés à étayer les évaluations réglementaires et la validation des plantes médicinales utilisées traditionnellement. L'outil d'évaluation historique pragmatique (PHA) offre une méthode systématique et adaptable pour compiler et évaluer les indications thérapeutiques documentées dans les traditions médicales écrites, allant au-delà de celles actuellement mises en avant dans les essais cliniques randomisés modernes. En intégrant les connaissances cliniques historiques et actuelles, l'outil PHA démontre son utilité pratique pour recenser un large éventail d'utilisations médicinales traditionnelles de longue date, afin d'éclairer les évaluations des allégations d'usage traditionnel. Bien qu'il ait été initialement appliqué à la materia medica européenne, l'outil PHA présente un potentiel significatif d'adaptation à d'autres traditions médicales codifiées.
Sandra Clair, PhD, est une scientifique de la santé et herboriste médicale agréée basée à Dunedin, en Nouvelle-Zélande, dont les recherches portent sur l'intégration des connaissances traditionnelles en matière de plantes médicinales dans les cadres réglementaires modernes. Elle a obtenu son doctorat en sciences de la santé à l'université de Canterbury à Christchurch, en Nouvelle-Zélande.
Ray Kirk, PhD, est professeur émérite à la Faculté des sciences de la santé de l'Université de Canterbury, à Christchurch, en Nouvelle-Zélande. Son expertise couvre l'évaluation des technologies de la santé, l'informatique de santé et la recherche sur les services de santé, avec un accent particulier sur les soins de santé fondés sur des données probantes.
Ian Douglass Coulter, PhD, est professeur émérite à l'Université de Californie à Los Angeles et chercheur principal en politique de santé à la RAND Corporation. Il est spécialisé dans la médecine complémentaire et intégrative ainsi que dans la recherche sur la prestation des soins de santé.
Reinhard Saller, PhD, MD, est professeur émérite à l'Université de Zurich en Suisse et un expert de premier plan en phytothérapie et en médecine intégrative. Ses travaux portent sur l'évaluation clinique et les données probantes relatives aux plantes médicinales.